К какому классу соединений относится этиленгликоль: Этиленгликоль — какой класс веществ?
Этиленгликоль — какой класс веществ?
Промывка- Промывка
- Промывка труб отопления
- Промывка теплоносителей
- Промывка кондиционера
- Промывка вентиляции
- Промывка пластинчатых теплообменников
- Промывка систем холодоснабжения
Этиленгликоль относится к классу многоатомных спиртов, причем это один из самых простых представителей полиолов. Химическая формула у него элементарная, поскольку в состав входит мало компонентов. Если вас интересуют более точные данные по вопросу “этиленгликоль, какой класс веществ”, мы ответим, что это двухатомный спирт и приведем формулу.
Как видите, в составе вещества всего три химических элемента и они находятся в предельно ясных “взаимоотношениях”.
Ну конечно, ответ на вопрос будет неполным, если мы не расскажем об основных физических и химических свойствах этиленгликоля. Это мы и спешим сделать.
Характеристики этиленгликоля
Это бесцветная жидкость без запаха, имеющая консистенцию сиропа, сладковатая на вкус, хотя пробовать ее настоятельно не рекомендуем, иначе не избежать серьезного отравления. Некоторые по незнанию хотят с ее помощью достичь состояния, подобного алкогольному опьянению, но такие эксперименты чреваты тяжелейшими состояниями.
Этиленгликоль ядовит. Принимать внутрь его нельзя. Смертельная доза, в зависимости от индивидуальной непереносимости, составляет от 50 миллилитров до 500 миллилитров, в среднем 100 миллилитров.
Этиленгликоль прекрасно растворяется в воде, спирте или ацетоне, плохо — в хлороформе или бензине. Принимает участие во всех химических реакциях, что и одноатомные спирты.
Вещество не горючее и слабо разлагается под воздействием света. Воспламеняется при температуре 124 градуса. Самовоспламеняется по достижении 380 градусов. Температура кипения — 197,3 градуса.
История и применение этиленгликоля
Это вещество впервые было получено в 1859 году французским химиком Шарлем Адольфом Вюрцем путем омыления диацетата этиленгликоля гидроксидом калия. Чуть позже применялись другие способы изготовления: добавление гидроксида к этиленгликольдиацетату и гидрирование этиленоксида.
Применение этиленгликоль нашёл не сразу. Впервые его начали производить на промышленном уровне только в 1917 году в США.
В 1929 году многие производители динамита стали активно использовать это вещество, а во время Первой мировой войны в Германии его применяли для изготовления взрывчатых веществ.
Сегодня этиленгликоль активно используют в автомобильной отрасли (антифризы, гидравлические жидкости), авиации, газодобывающей промышленности, в качестве энергоносителей. Современное производство нашло широкое применение простейшему многоатомному спирту, который легко получить в химической лаборатории. Качественный продукт всегда сбывают быстро.
Интересные статьи
Этиленгликоль — это… Что такое Этиленгликоль?
Этиленглико́ль (гликоль; 1,2-диоксиэтан; этандиол-1,2), HO—CH2—CH2—OH — простейший представитель полиолов (многоатомных спиртов). В очищенном виде представляет собой прозрачную бесцветную жидкость слегка маслянистой консистенции. Не имеет запаха и обладает сладковатым вкусом. Токсичен. Попадание этиленгликоля или его растворов в организм человека может привести к необратимым изменениям в организме и к летальному исходу [1].
История открытий и производства
Этиленгликоль впервые был получен в 1859 французским химиком Вюрцом из диацетата этиленгликоля омылением гидроксидом калия и в 1860 гидратацией этиленоксида. Он не находил широкого применения до Первой мировой войны, когда в Германии его стали получать из дихлорэтана для использования в качестве замены глицерина при производстве взрывчатых веществ. В США полупромышленное производство начато в 1917 году через этиленхлоргидрин. Первое крупномасштабное производство начато с возведением завода в 1925 году около Южного Чарлстона (западная Вирджиния, США) компанией «Carbide and Carbon Chemicals Co.» К 1929 году этиленгликоль использовался практически всеми производителями динамита. В 1937 кампания Carbide начало первое крупномасштабное производство, основанное на газофазном окислении этилена до этиленоксида. Монополия компании Carbide на данный процесс продолжалась до 1953 года.
Получение
В промышленности этиленгликоль получают путём гидратации оксида этилена при 10 атм и 190—200°С или при 1 атм и 50—100°С в присутствии 0,1—0,5 % серной или ортофосфорной кислоты, достигая 90% выхода. Побочными продуктами при этом являются этиленгликоль, триэтиленгликоль и незначительное количество высших полимергомологов этиленгликоля.
Применение
Благодаря своей дешевизне этиленгликоль нашёл широкое применение в технике.
- Как компонент автомобильных антифризов и тормозных жидкостей, что составляет 60 % его потребления. Смесь 60 % этиленгликоля и 40 % воды замерзает при −45 °С. Коррозионно активен, поэтому применяется с ингибиторами коррозии;
- В качестве теплоносителя в виде раствора в автомобилях, в системах жидкостного охлаждения компьютеров;
- В производстве целлофана, полиуретанов и ряда других полимеров. Это второе основное применение;
- Как растворитель красящих веществ;
- В органическом синтезе:
- в качестве высокотемпературного растворителя.
- для защиты карбонильной группы путём получения 1,3-диоксалана. Обработкой вещества с карбонильной группой в бензоле или толуоле этиленгликолем в присутствии кислого катализатора(толуолсульфоновой кислоты, насадке Дина-Старка образующейся воды. Например, защита карбонильной группы изофорона
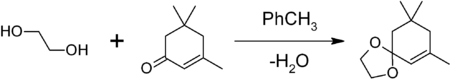
1,3-диоксоланы могут быть получены также при реакции этиленгликоля с карбонильными соединениями в присутствии триметилхлорсилана[2] или комплекса диметилсульфат-ДМФА[3] 1,3-диоксалана устойчивы к действию нуклеофилов и оснований. Легко регенерируют исходное карбонильное соединение в присутствии кислоты и воды.
- Как компонент жидкости «И», используемой для предотвращения обводнения авиационных топлив.
- В качестве криопротектора
- Для поглощения воды, для предотвращения образования гидрата метана, который забивает трубопроводы при добыче газа в открытом море. На наземных станциях его регенириуют путём осушения и удаления солей.
- Этиленгликоль является исходным сырьём для производства взрывчатого вещества нитрогликоля.
Этиленгликоль также применяется:
Очистка и осушение
Осушается молекулярным ситом 4А, полуводным сульфатом кальция, сульфатом натрия, Mg+I2, фракционной перегонкой под пониженным давлением, азеотропной отгонкой с бензолом. Чистота полученного продукта легко определяется по плотности.
Таблица плотности водных растворов этиленгликоля, 20°С
| Концентрация % | 30 | 35 | 40 | 45 | 50 | 55 | 60 |
|---|---|---|---|---|---|---|---|
| Плотность, г/мл | 1,050 | 1,058 | 1,067 | 1,074 | 1,082 | 1,090 | 1,098 |
Меры безопасности
Этиленгликоль — горючее вещество. Температура вспышки паров 120 °C. Температура самовоспламенения 380 °C. Температурные пределы воспламенения паров в воздухе, °С: нижний — 112, верхний — 124. Пределы воспламенения паров в воздухе от нижнего до верхнего, 3,8- 6,4 % (по объему). Требования безопасности Этиленгликоль горюч, по степени воздействия на организм относится к веществам 3-го класса опасности. Этиленгликоль токсичен. Летальная доза при однократном пероральном употреблении составляет 100—300 мл этиленгликоля (1,5-5мл на 1 кг массы тела)[4]. Имеет относительно низкую летучесть при нормальной температуре, пары обладают не столь высокой токсичностью и представляют опасность лишь при хроническом вдыхании. Определённую опасность представляют туманы, однако при их вдыхании об опасности сигнализируют раздражение и кашель. Противоядием при отравлении этиленгликолем являются этанол и 4-метилпиразол (англ.
См. также
Примечания
Ссылки
формула, свойства, получение, применение и класс опасность
Глицерин и этиленгликоль (ethylene glycol) являются самыми известными химическими веществами, которые применяют в различных сферах деятельности. Их исследование несколько веков назад показало, что схожих веществ не существует. Многоатомные спирты используют и в химических синтезах, и в отраслях промышленности, и в сферах человеческой деятельности.
Однако эти вещества имеют и отрицательные качества. Поэтому стоит тщательно разобрать состав этиленгликоля, его формулу и степень опасности для человека.


Что такое этиленгликоль
По определению этиленглико́ль (гликоль, 1,2-диоксиэтан, этандиол-1,2) — кислородсодержащее органическое соединение, двухатомный спирт, простейший представитель многоатомных спиртов. Если вещество очищено, то представляет собой прозрачную бесцветную жидкость маслянистой консистенции.
Изначально этиленгликоль использовался во времена Первой мировой войны в качестве глицерина. Однако со временем изменил свое направление. Его стали использовать в различных сферах химической промышленности.


Формула и класс вещества
Химическая формула гликоля — C2H6O2, рациональная — C2h5 (OH) 2, структурная — HO—Ch3—Ch3—OH . В основе молекулы лежит непредельный скелет этилена, который состоит из двух атомов карбона. На свободные валентные места присоединились две гидроксильные группы.
У этиленгликоля есть несколько названий, которые зачастую встречаются в составе продуктов химического производства:
- гликоль;
- этандиол-1,2;
- 1,2-диоксиэтан.
Молекула имеет подобие транс-конфигурации в размещении гидроксильных групп. Такое расположение соответствует самому удаленному расположению водородов, что дает максимальную устойчивость системы.
Как получают
Массовое получение 1.2-этандиола началось еще в тридцатые годы прошлого века. Сначала получали лишь одним методом, потом появились новые. Таким образом, гликоль можно получить несколькими способами, однако некоторые из них стали частью истории, а другие превзошли их качеством.
Изначально 1,2-диоксиэтан получали из дибромэтана. Двойная связь этилена разрывается, а свободные валентности занимаются галогенами — исходным веществом в данной реакции. Образование промежуточного соединения возможно благодаря замещению ацетатными группами, которые при гидролизе превращаются в спиртовые.
С улучшением технологий появился новый метод — получение этиленгликоля прямым гидролизом любых этанов и этиленов , которые замещены двумя галогенами соседних атомов карбона. С помощью различных водных растворов, карбонатов металлов, воды и диоксида свинца начинается реакция, которая возможна лишь при больших температурах и давлении. Побочные вещества — диэтиленгликоль и триэтиленгликоль.
Следующий способ позволил получать 1,2-диоксиэтан из эфира этиленхлоргидрина путем его гидролиза угольными солями. При 170 градусах выход целевого продукта достигал 90 %. Однако был значительный недостаток — гликоль необходимо извлекать из раствора соли. Ученые решили эту проблему. Они разбили процесс на две стадии, при этом оставив то же исходное вещество.
Гидролиз этиленгликоль ацетатов стал отдельным способом, когда получилось добыть исходный реагент путем окисления этилена в уксусной кислоте кислородом.


Свойства
1,2-диоксиэтан не имеет запаха, однако, имеет сладковатый вкус. Относят к умеренно токсичным легковоспламеняющимся веществам. Легко соединяется с водой. Это используют в промышленности, так как температура замерзания таких веществ очень низкая.
Физические
Еще в прошлом веке стало известно, что этиленгликоль обладает уникальными свойствами.
Характеристики:
- температура возгорания составляет от +112 ˚С до +124 ˚С;
- самовоспламениться может при нагреве до +380 ˚С;
- чистый этиленгликоль замерзает при -12 ˚С;
- раствор на водной основе может замерзать при температуре ниже -65 ˚С, а при более низком значении начинается образование кристаллов льда;
- точка кипения чистой жидкости достигается при +121 ˚С;
- плотность — 11,114 г/см³.
Такие характеристики дают возможность применять 1,2-диоксиэтан в различных сферах производства.
Химические
Вещество имеет несколько названий, но все они означают одно и то же. Собственно, и химические свойства у них одинаковы. Если массовая доля вещества достигает 99.8%, то оно высшего сорта.
Список химических свойств:
- молярная масса — 62,068 г/моль;
- коэффициент оптического преломления — 1,4318;
- константа диссоциации кислоты — 15,1±0,1;
- умеренно токсичный.
1.2-этандиол относят к третьей группе опасности, поэтому предельно допустимые концентрации в атмосфере по ГОСТу могут быть не более 5 миллиграмм/м³.


Применение
Этиленгликоль нашел свое призвание во многих отраслях. Незаменимым веществом является и в автомобилестроении. Его уникальные свойства позволяют создать высококачественные жидкости.
Может регенерировать исходное карбонильное соединение в присутствии воды и кислоты:
- Как компонент противоводокристаллизационной жидкости «И».
- В качестве криопротектора.
- Для поглощения воды, предотвращения образования гидрата метана, который забивает трубопроводы при добыче газа в открытом море. На наземных станциях его регенерируют путем осушения и удаления солей.
- Этиленгликоль является исходным сырьем для производства взрывчатого вещества нитрогликоля.
1,3-диоксоланы могут быть получены при реакции этиленгликоля с карбонильными соединениями в присутствии триметилхлорсилана. Такие соединения устойчивы к действию нуклеофилов и оснований.
В автомобилях
Благодаря своей дешевизне этиленгликоль нашел широкое применение в технике.
Он может быть использован:
- как компонент тормозных жидкостей и автомобильных антифризов;
- как теплоноситель с содержанием не более 50 % в системах отопления;
- в качестве теплоносителя в виде раствора в автомобилях и системах жидкостного охлаждения компьютеров;
- в производстве полиуретанов, целлофана и ряда других полимеров;
- как растворитель красящих веществ;
- в качестве высокотемпературного растворителя.
- для защиты карбонильной группы путем получения 1,3-диоксолана.
Наиболее известное его направление — компонент автомобильных антифризов. Эта отрасль составляет 60 % его потребления. Такие смеси могут не замерзать при низких температурах, а также коррозийно устойчивы.


В других отраслях
Кроме того 1,2-диоксиэтан является незаменим и в других отраслях промышленности.
1.2-этандиол также применяется:
- при производстве конденсаторов;
- при производстве 1,4-диоксана, пропиленгликоля;
- как теплоноситель в системах чиллер-фанкойл;
- в качестве компонента крема для обуви;
- в составе для мытья стекол вместе с изопропиловым спиртом;
- при криоконсервировании биологических объектов в качестве криопротектора;
- при производстве полиэтилентерефталата, пластика.
И хотя 1,2-диоксиэтан применяют в других отраслях, их процент применения довольно мал.


Вред для человека
Однако 1.2-этандиол имеет и свои минусы. Неряшливое или неаккуратное его использование может привести к трагическим последствиям.
Класс опасности вещества
Класс опасности этиленгликоля — третья группа, то есть его контакт с окружающей средой должен быть как можно меньше. Если же 1.2-этандиол попадает в организм человека, в нем могут развиться необратимые негативные явления. При однократном употреблении внутрь 100 и более миллилитров наступает летальный исход.
Пары данного вещества же менее токсичны, однако систематическое вдыхание может привести к гибели. Если человек отравляется гликолем, ему следует принять препарат, который содержит 4-метилпиразол.


Симптомы отравления
В воспалительный процесс вовлекаются все системы органов. Скрытый период отравления этиленгликолем обычно равен 12 часам, но сроки могут изменяться в зависимости от количества употребленного спирта.
Симптомы отравления:
- Первый период проявляется всего несколько часов, но не более 12. Характеризуется легким опьянением. Появляется незначительная слабость и невнятная речь, но в целом самочувствие нормальное. В редких случаях беспокоит тошнота, периодическая рвота и боли в животе. От отравленного человека исходит сладковатый запах.
- Через 12 часов после отравления возникает головокружение и головные боли, жажда и тошнота. Появляется рвота, сильнейшие боли в желудке, боль в пояснице и мышцах.
- Немного позже появляются признаки поражения нервной системы: возбуждение и потеря сознания, многочисленные судороги, повышается температура тела. Отравление этиленгликолем проявляется нарушением работы сердца и сосудов: увеличивается частота биения, снижается артериальное давление.
- Нарушается работа дыхательной системы: постепенно появляется одышка, поверхностное дыхание и отек легких. Тяжелые больные теряют сознание.
- Приблизительно на пятые сутки развивается нарушение в работе печени и почек. Из-за почечной недостаточности возможен летальный исход в течение одной недели.
- Если произошло острое отравление, то наступает смерть из-за паралича дыхательного центра и отека легких.
Легкое отравление возможно при вдыхании паров 1.2-этандиола. Симптомами являются легкая тошнота, слабость.


Меры предосторожности при работе с этиленгликолем
Этиленгликоль является горючем веществом. Температурные пределы воспламенения паров в воздухе начинаются от 112 и заканчиваются 124 °С. Пределы воспламенения паров в воздухе от нижнего до верхнего — 3,8‒6,4 % от объема.
Летальная доза при однократном пероральном употреблении — 100‒300 мл этиленгликоля. Имеет относительно низкую летучесть при нормальной температуре. Опасность представляют туманы, однако при их вдыхании об опасности сигнализируют раздражение и кашель. П ри отравлении следует принять препараты, содержащие этанол или 4-метилпиразол.


Видео о получении вещества
В следующем видео расскажут о получении гликоля.
что такое, применение, отравление — симптомы, первая помощь, лечение, профилактика
 Один из типичных представителей спиртов — это этиленгликоль. Эта жидкость входит в состав многих химических средств в том числе для ухода за машинами и помещениями. Но так как этиленгликоль имеет непосредственное отношение к спиртам — его периодически пытаются выпить как заменитель алкоголя. Не все знают, что именно этот представитель обладает наиболее выраженными отравляющими качествами.
Один из типичных представителей спиртов — это этиленгликоль. Эта жидкость входит в состав многих химических средств в том числе для ухода за машинами и помещениями. Но так как этиленгликоль имеет непосредственное отношение к спиртам — его периодически пытаются выпить как заменитель алкоголя. Не все знают, что именно этот представитель обладает наиболее выраженными отравляющими качествами.
Что такое этиленгликоль, какая у него формула и физические свойства? Как его получают и где применяют? Чем опасен для организма человека этот спирт? В каких случаях происходит отравление им и что за симптомы беспокоят при этом? Как нужно действовать, чтобы помочь пострадавшему?
Что такое этиленгликоль
Этиленгликоль — это представитель спиртов с двумя метильными группами в своём составе. Но в отличие от других он имеет немного маслянистую консистенцию.
Несмотря на то что этиленгликоль был получен ещё в 1859 году, он не сразу занял свою нишу в химии и промышленности. Изначально он использовался во времена Первой мировой войны, как замена глицерина, который широко применялся при производстве взрывчатых веществ.
Химическая формула этиленгликоля — C2H6O2, рациональная — С2Н4(ОН)2. По своим физическим свойствам — это жидкость без запаха, но со сладким вкусом. Он легко соединяется с водой в любой консистенции, что успешно применяется в промышленности, ведь температура замерзания таких жидкостей очень низкая — это улучшает свойства «незамерзаек».
- гликоль;
- этандиол-1,2;
- 1,2-диоксиэтан.
Чаще других употребляется основное название.
К какому классу опасности относится этиленгликоль? — к умеренно токсичное легковоспламеняющееся вещество.
Способы получения
Производством этиленгликоля в промышленных масштабах занялись ещё в тридцатые годы прошлого века. Одним из способов его получения тогда было окисление этилена до его оксида. Около 20 лет такой метод оставался единственным.
Немного позже этиленгликоль стали получать с помощью насыщения оксида этилена водой, в присутствии серной и ортофосфорной кислот. Этот способ оказался выгодней предыдущего, так как на выходе производили более 90% этиленгликоля с минимальным количеством примесей.
Где применяется
В основном этиленгликоль используют в промышленности для обработки техники, что обусловлено его стоимостью — это недорогой и всем доступный продукт.
 Он выпускается в химической промышленности для ухода за автомобилями:
Он выпускается в химической промышленности для ухода за автомобилями:
- более 50% вещества идёт на создание тормозных жидкостей и антифризов, так как смесь гликоля и воды способна сохранять жидкую консистенцию даже при 40º C ниже нуля;
- этиленгликоль входит в состав охлаждающей жидкости — тосола;
- он может устранять коррозию, поэтому гликоль добавляют в антикоррозийные химические соединения.
Где ещё используется этиленгликоль?
- Его можно обнаружить в составе антистатиков.
- Используют для производства средств защиты против обледенения.
- Служит смазкой в холодильных установках.
- Находит применение этиленгликоль как наполнитель в гидравлических системах.
- Гликоль нередко используют для дезинфекции больших помещений.
- Одно из ключевых применений вещества — это производство бытовых химических продуктов, к числу которых относится целлофан, полиуретан.
- Он используется не только при охлаждении автомобилей, но и компьютеров.
- Этиленгликоль или химические соединения в составе с ним применяется, как средство для чистки автомобильных стёкол и зеркал.
 В небольшом количестве присутствует в креме для обработки обуви.
В небольшом количестве присутствует в креме для обработки обуви.- Применяется этиленгликоль и в медицине, как составная часть криопротекторов для тканей и органов. То есть веществ, которые используют для заморозки.
- Это один из компонентов конденсаторов.
- Ключевым свойством этиленгликоля является поглощение воды, что успешно используется, чтобы предотвратить обледенение топлива в авиации и синтеза гидрата метана в трубопроводах, которые проходят в море.
- В органической химии его применяют как высокотемпературный растворитель.
- Без него не проходит синтез химических соединений.
- Где ещё используется этиленгликоль? — даже в наше время с его участием создают взрывчатые вещества.
За прошедшие десятилетия для этого двухатомного спирта нашлось множество применений, что, конечно же, обусловлено его свойствами. Но в медицине он известен не только как полезный и нужный продукт в быту, но и как средство, после контакта с которым человек может умереть.
Так что это такое этиленгликоль? — полезное химическое вещество, без которого не обходится производство большинства органических соединений или сильнодействующий яд с мощным отравляющим эффектом? Давайте узнаем, как может повлиять этиленгликоль на человека.
Влияние этиленгликоля на организм человека
Этот двухатомный спирт в основном входит в состав продуктов для ухода за помещениями, машинами и техникой. По своим физическим свойствам он отличается от привычного спирта маслянистой консистенцией и отсутствием запаха, поэтому его сложно перепутать с этанолом или изопропанолом, которые нередко употребляют внутрь. Возможны ли отравления этиленгликолем у людей? — да, несмотря на явные различия с другими спиртами отравиться им можно.
В каких случаях происходит отравление?
 Этиленгликоль является одним из средств обработки больших помещений. Во время нанесения моющих средств его пары вдыхаются, а при нарушении техники безопасности небольшое количество соединения может попасть в рот. Хотя для отравления этого недостаточно.
Этиленгликоль является одним из средств обработки больших помещений. Во время нанесения моющих средств его пары вдыхаются, а при нарушении техники безопасности небольшое количество соединения может попасть в рот. Хотя для отравления этого недостаточно.- Гликоль попадает внутрь при постоянной работе с ним, к примеру, если человек трудится на химическом производстве продуктов, содержащих этиленгликоль.
- Отравиться можно при случайном употреблении его внутрь.
- Так как это химическое соединение используется для обработки машин, то в группе риска находятся люди, регулярно сталкивающиеся с ним по долгу службы.
Этиленгликоль токсичен и относится к веществам третьего класса опасности. После поступления в организм человека он очень быстро всасывается в желудке и верхнем отделе тонкого кишечника. Не более 30% его выделяется в неизменном состоянии почками или в виде солей. Остальная же часть поступает в печень, где и происходит его преобразование.
В печени он разлагается до конечных продуктов:
- гликолевой кислоты;
- муравьиной и щавелевой кислоты;
- гликолевого альдегида.

Как влияет этиленгликоль на организм человека? Все эти конечные продукты распада действуют на кислотно-щелочное равновесие, что постепенно приводит к некрозу клеток головного мозга и почечной ткани. В организме развивается ацидоз или увеличение кислотности. Смертельная доза для человека составляет всего 100–150 мл. Но даже попадание небольшого количества этиленгликоля приведёт к развитию отравления, хотя и в лёгкой степени.
Симптомы отравления
В воспалительный процесс после употребления этиленгликоля вовлекаются не только почки и головной мозг. Спирт и его конечные продукты влияют на все системы органов. Скрытый период отравления этиленгликолем в среднем равен 12 часов, но он может укорачиваться или удлиняться в зависимости от количества употреблённого спирта.
 Какие симптомы отравления?
Какие симптомы отравления?
- Первый период (начальный) проявляется всего несколько часов, не более 12, и характеризуется лёгким опьянением. Человека беспокоит незначительная слабость и невнятная речь, но в целом самочувствие нормальное. В это время на отравление этиленгликолем указывает только необычный сладковатый запах, исходящий от человека. В редких случаях беспокоит тошнота, периодическая рвота, боли в животе.
- Спустя 12 часов после периода мнимого благополучия, возникает головокружение, головные боли, жажда и тошнота.
- К симптомам отравления этиленгликолем в это время относятся рвота, сильнейшие боли в желудке, которые напоминают признаки острого живота, боль в пояснице и мышцах.
- Немного позже на первое место выходят признаки поражения нервной системы: возбуждение и потеря сознания, появляются многочисленные судороги, увеличивается температура тела.
- Отравление этиленгликолем проявляется ещё и нарушением работы сердца и сосудов: увеличивается частота биения, снижается артериальное давление.
- Нарушается работа дыхательной системы: постепенно появляется одышка, поверхностное дыхание и отёк лёгких.
 Тяжёлые больные теряют сознание.
Тяжёлые больные теряют сознание.- Приблизительно на пятые сутки развивается нарушение в работе почек и печени. Из-за почечной недостаточности летальный исход наблюдается в течение одной недели.
- Смерть наступает в первые дни острого отравления из-за паралича дыхательного центра, отёка лёгких и вследствие сердечно-сосудистой недостаточности.
Лёгкое отравление этиленгликолем наблюдается чаще при вдыхании его паров небольшой концентрации. Оно проявляется незначительными симптомами: слабостью, подташниванием, головокружением.
Первая помощь при отравлении
К сожалению, часто причиной запоздалой или несвоевременной помощи становится лёгкое течение отравления, хроническая интоксикация парами этого спирта или позднее обращение пострадавшего человека к медработникам. В этом случае продукты распада гликоля уже оказывают своё повреждающее действие на внутренние органы и наносят непоправимый ущерб здоровью.

этанол — антидот при отравлении этиленгликолем
Что можно сделать на доврачебном этапе, чтобы помочь пострадавшему? Для этого необходимо быть уверенным в употреблении именно этого вещества. Если этиленгликоль был выпит недавно — нужно незамедлительно промыть желудок и ввести слабительное. Активированный уголь не окажет выраженного эффекта.
Быстро помочь при отравлении этиленгликолем, может, антидот — этанол. В этом случае применяется во внутрь его 30%-й раствор или 5%-й вводится внутривенно. А также в качестве антидота используется кальция хлорид или глюконат 10%-й раствор внутривенно или внутрь.
Не у всех под рукой могут оказаться нужные лекарства для оказания экстренных мероприятий. В этом случае неотложная помощь при отравлении этиленгликолем заключается во введении через зонд или рот обычной водки.
Если человек без сознания — его нужно уложить набок и дать доступ кислорода — открыть окно, развязать галстук и освободить от стягивающей одежды.
До момента начала активных действий нужно вызвать бригаду скорой помощи, так как пострадавшему понадобится госпитализация.
При отравлении этиленгликолем у детей нужно действовать незамедлительно и как можно скорее доставить пострадавшего малыша в ближайшую больницу!
Лечение отравления в стационаре
После госпитализации больному человеку проводят курс интенсивной терапии. Если пострадавшему не был дан антидот бригадой скорой помощи, то по прибытии в стационар его вводят сразу же.
Дальше лечение заключается в применении симптоматических препаратов для коррекции работы жизненно важных органов и систем.
 При отравлении этиленгликолем пострадавшему обеспечивают физический покой, доступ кислорода.
При отравлении этиленгликолем пострадавшему обеспечивают физический покой, доступ кислорода.- Назначают витамины группы B и C, АТФ (аденозинтрифосфорная кислота).
- При необходимости вводят преднизолон.
- При отравлении этиленгликолем назначают в большом количестве фолиевую кислоту, чтобы связать продукты распада этого двухатомного спирта.
- Вводят солевые растворы.
Профилактика отравления
Какая должна быть профилактика отравления этиленгликолем?
 При работе с химическими веществами, содержащими этиленгликоль, нужно использовать индивидуальные средства защиты.
При работе с химическими веществами, содержащими этиленгликоль, нужно использовать индивидуальные средства защиты.- Не стоит пить подозрительные жидкости.
- Хранить в недоступном для детей месте все химикаты для защиты и обработки машины, а также уборки помещений.
Этиленгликоль — насколько опасно это соединение? Нельзя недооценивать его негативное влияние на организм человека. Симптомы отравления, при попадании спирта внутрь, развиваются практически молниеносно, а смерть может наступить, спустя всего 5 дней. Отравление этиленгликолем очень легко предупредить и вылечить, если известно, что человек выпил. В противном случае терапия затягивается надолго.
Этиленгликоль
Этиленгликоль – прозрачная жидкость, двухатомный спирт, является одним из полиолов. Это жидкость, не обладающая запахом и цветом, сладковата на вкус. Незначительная доза этиленгликоля способна вызвать при принятии внутрь необратимые последствия, вплоть до летального исхода. Согласно традиционной химической номенклатуре, этиленгликоль называют 1,2-диоксиэтаном либо 1,2-этандиолом.
Синтез этиленгликоля
Первую реакцию, продуктом которой является этиленгликоль связывают с именем французского химика Вюрца. В конце пятидесятых годов XIX века он произвёл омыление калийной щелочью диацетата этиленгликоля, в ходе которой и получился вышеописанный многоатомный спирт. Так как в тот период времени его свойства были изучены недостаточно, в течение долгого времени этиленгликоль не считался полезным и только с началом Первой мировой войны немецкие учёные догадались заменить им глицерин в военно-промышленном комплексе, в частности, в производстве взрывчатки. Данный способ также был усовершенствован и 1,2-этандиол стал продуктом реакции гидролиза дихлорэтана с присутствием щелочи.
В настоящее же время самой рациональной и выгодной реакцией для получения этиленгликоля считается присоединение молекулы воды к оксиду этилена при давлении в 10 атмосфер и средней температуре либо при высоком температурном показателе с наличием раствора ортофосфорной кислоты малой концентрации (до 0,5%).
Использование этиленгликоля в хозяйственной деятельности
Помимо опасного применения этиленгликоля при создании взрывчатых материалов, у 1,2-этандиола есть более «повседневные» задачи. Например, ввиду весьма дешевого способа промышленного производства, ему нашли применение в технике. Благодаря низкой температуре замерзаний (менее -49 градусов Цельсия) его используют при производстве практически любого антифриза или тормозной жидкости. По статистике, около 60% произведенного этиленгликоля используется именно в этой отрасли. Также этиленгликоль используется в качестве теплоносителя в отопительных и кондиционирующих системах зданий, широко применяется в жидкостном охлаждении компьютеров. Следующими основными потребителями этиленгликоля являются заводы по производству полимерных материалов, таких как целлофан и полиуретан. Используется он также как растворитель в красках, лаках и некоторых видах синтеза органических соединений, является одной из составляющих противоводокристаллизационной жидкости, которая входит в число компонентов автомобильного топлива и служит.
Основной задачей этой жидкости является препятствование образованию частичек льда в условиях никого температурного показателя. 1,2-этандиол применяется как защитник карбонильной группы в ходе превращения этиленгликоля и карбонильных соединений в 1,3-диоксолан в присутствии, например, диметилформамида (диметилсульфат-ДМФА). В трубопроводах данное вещество применяется как ингибитор гидратообразования (препятствует появлению метангидрата – соединения метана с водой, которое из-за своей устойчивости в условиях нефтегазового трубопровода может нарушить работу морских нефтяных платформ).
Этиленгликоль часто является сырьем в производстве взрывоопасного вещества этиленгликольдинитрата, но и этим его применения не ограничиваются. Помимо вышеперечисленного, его активно применяют при сборке конденсаторов, производстве полиэтилентерефталата (пластика, из которого изготавливаются бутылки), кремов для обуви, стеклоочистных составов, синтезе 1,4-диоксана, крионике (как вещество, защищающее биологическую ткань от повреждений при экстремально маленькой температуре вплоть до заморозки) и т. д.
Рекомендации по безопасной работе с этиленгликолем
Учитывая тот факт, что этиленгликоль взрыво- и огнеопасен (в центре вспышки его паров достигается температура 120 C, а при горении – 380 C) хранить его стоит в герметизированной посуде, не допускающей утечки самого вещества или проникновения внутрь горячих продуктов.
Этиленгликоль – достаточно токсичное соединение, способное при разовом употреблении 100-300 мл вызвать летальный исход. Эти параметры соответствуют веществам 3-го класса опасности по воздействию на организм. Пары соединения представляют опасность при регулярном их вдыхании, поэтому при работе с 1,2-диоксиэтаном настоятельно рекомендуется использовать индивидуальные средства защиты дыхательных путей и кожных покровов. Сигналом опасности могут послужить кашель и раздражение. При попадании на поверхность или кожу, в отличие от кислот, которые сильно разогреваются при смешивании с водой, этиленгликоль при разбавлении не вступит в экзотермическую реакцию (с обильным выделением тепла), поэтому его можно смывать водой.
Этиленгликоль в организме человека
Содержание этиленгликоля в человеческом организме невелико. При его окислении до щавелевой кислоты у человека могут возникнуть проблемы с почками, однако более частым путём метаболизирования этиленгликоля является его окисление до гликолевой кислоты с последующим распадом до диоксида углерода.
Использование рефрактометров в исследовании этиленгликоля
Для того, чтобы проанализировать качество конкретного образца 1,2-этандиола и определить его дальнейшее назначение используют рефрактометры. Это приборы, функционирование которых основано на анализе оптических свойствах среды, фиксируют показатель преломления исследуемого образца и, исходя из полученных данных, определяют концентрацию раствора и температуру замерзания теплоносителя (коим чаще всего выступает этиленгликоль).
Этиленгликоль — класс опасности и основные характеристики
Промывка- Промывка
- Промывка труб отопления
- Промывка теплоносителей
- Промывка кондиционера
- Промывка вентиляции
- Промывка пластинчатых теплообменников
- Промывка систем холодоснабжения

Этиленгликоль — базовое вещество, используемое для производства антифризов и теплоносителей (класс опасности этиленгликоля — 3). Благодаря его отличительным параметрам, материалы на его основе эффективны для работы в транспортных системах, в оборудовании, применяемом для охлаждения и отопления. Главное, что стоит помнить, при работе с растворами — этиленгликоль вреден для человека, он токсичен. Требуется особая осторожность и внимательность при обращении.
Особенности этиленгликоля
Этот материал классифицируют как вещество третьей группы опасности. Класс опасности этиленгликоля говорит о способе транспортировки и хранении. Растворы с его содержанием перевозят в специализированных емкостях, оцинкованных резервуарах, которые герметично закрыты. Можно перевозить и в автоцистернах, только их нужно подготовить для этих целей. Водитель должен следовать инструкции во время доставки раствора, чтобы избежать разгерметизации ёмкости.
Этиленгликоль — бесцветная жидкость, не имеющая запаха, обладающая слегка сладковатым вкусом и маслянистой структурой. Физические характеристики дают возможность применять вещество в производстве.
- Температура возгорания составляет от +112 ˚С до +124 ˚С.
- Самовоспламениться может при нагреве до +380 ˚С.
- Чистый этиленгликоль замерзает при -12 ˚С.
- Раствор на водной основе вместе с дополнительными присадками может замерзать при температуре ниже -65 ˚С.
- При более низком значении начинается образование кристаллов льда.
- Точка кипения чистой жидкости достигается при +121 ˚С.
- Плотность — 11,114 г/куб. см.
Сфера применения
Этиленгликоль может использоваться не только как антифриз, его применяют в промышленности в разных сферах.
- В качестве растворителя для красящих соединений.
- Для производства нитрогликоля — взрывчатого материала.
- В газодобывающей промышленности. Этиленгликоль необходим для формирования гидрата метана в трубопроводе. Кроме этого, вещество поглощает лишнюю воду в трубах.
Чем опасен этиленгликоль?
Материалы, которые относятся к третьей группе опасности (среди них и этиленгликоль) необходимо хранить в герметичных емкостях. Их контакт с окружающей средой должен быть минимизирован. Человеку опасно находиться при концентрации этого вещества в атмосфере больше 5 миллиграмм/метр кубический. Отличительные особенности при постоянном попадании этиленгликоля в организм:
- слабость;
- сонливость;
- вялость;
- в тяжелых случаях — потеря сознания.
Постоянное вдыхание паров эфира приводят к развитию вегетососудистой дистонии.
Все сотрудники, которые имеют отношение к химическому производству и к работе с токсическими веществами третьего класса опасности, должны строго соблюдать все правила техники безопасности. В противном случае не исключен и летальный исход.
На производстве работают в специальных костюмах, надевая:
- респиратор соответствующего класса защиты;
- бахилы;
- халат;
- очки.
Важно закрыть все открытые участки тела и предотвратить попадание паров в дыхательные органы.
Длительность работы раствора
Раствор на базе этиленгликоля может работать в течение 5 лет, не теряя своих характеристик. Затем жидкость подлежит замене. Для того, чтобы определить, когда вещество подлежит замене, проводятся специальные исследования. На основе результатов принимается соответствующее решение. Делают целый ряд тестов, в которых проверяются характеристики рабочей жидкости. Если раствор утратил часть своих свойств, его нужно заменить, чтобы восстановить эффективность работы всей системы и не привести к повреждению отдельных элементов теплообменника. Купить раствор этиленгликоля в воде можно на нашем сайте.
Интересные статьи
Тест по теме: «Спирты. Фенолы.» 10 класс
Спирты. Фенолы. Вариант № 1
1.К какому классу соединений относится глицерин:
Одноатомные спирты 2. Простые эфиры 3. Многоатомные спирты 4. Альдегиды
2.Какое соединение образуется при взаимодействии этилового спирта и бутановой кислоты:
1. С2Н5СООС2Н5 2. СН3СООС3Н7 3. С3Н7СООС2Н5 4. С3Н7СОС2Н5
3.Укажите вещество Х3 в схеме СН3СН2ОН Н2SO4,t → Х1 HCI → Х2 Na,t→ Х3
1.Ацетилен 2. Бутан 3. Этан 4. 2-бутен
4. Гидроксид натрия при нормальных условиях образует соль при взаимодействии с:
1. Фенолом 2. Этанолом 3. Уксусным альдегидом 4. Анилином
5. Перевод С2Н4 → С2Н5ОН осуществляется реакцией:
1. Гидратация 2. Гидрирование 3. Дегидратация 4. Горения
6. Качественной реакцией на этиленгликоль является его взаимодействие с:
1. Си(ОН)2 2. Ва(ОН)2 3. Си 4.СН3СООН
7. Сложные эфиры – это продукты взаимодействия:
1. Спирта с альдегидом 2. Двух спиртов 3. Алкенов с водой 4. Кислот со спиртами
8. С2Н5ОNа можно получить взаимодействием этанола с:
1. Na 2. NaOH 3. NaCI 4. NaH
9. В молекуле СН3ОNа имеются следующие виды химической связи:
1. Только ковалентная 2. Ковалентная полярная и ковалентная неполярная
3. Только ионная 4. Ковалентная полярная и ионная
10. В схеме превращений С2Н6 → А → С2Н5ОН веществом «А» является:
1. Хлорэтан или этилен 2. Только хлорэтан 3. Только этилен 4. Ацетальдегид
11. Глицерат меди (II) можно получить взаимодействием глицерина при обычных условиях с:
1. Си 2. СиО 3. Си(ОН)2 4. СиСI2
12. Как называется вещество: СН3 СН3 СН3
СН3 – СН – СН — СН2 —С – СН2ОН
СН3
1.2,3,5,5 –тетраметилгексанол-6 2. 2,2,4,5-тетраметилгексанол-1 3. 2,3,5,5-тетраметилгексанол -1 4. 2,3,5,5-тетраэтилгексанол-1
13 . Укажите формулу гомолога фенола:
1. С6Н5ОН 2. С7Н7ОН 3. С8Н17ОН 4. С9Н17ОН
14. Как установить в какой пробирке этанол, а в какой – водный раствор фенола:
1. Действием активного металла 2. Действием бромной воды
3. Действием раствора щелочи 4. Действием лакмуса
15. Качественной реакцией на фенолы является образование окрашенных комплексов с раствором:
1. NaOH 2. HCI 3. FeCI3 4. CuSO4
16. Диметиловый эфир и этиловый спирт являются:
1. Структурными изомерами 2. Геометрическими изомерами
3. Гомологами 4. Одним и тем же веществом
17. Образование фенолформальдегидной смолы является реакцией:
1. Полимеризации 2. Поликонденсации 3. Сополимеризации 4. Соединения
18. Какое вещество имеет наиболее выраженные кислотные свойства:
1. Н2О 2. СН3ОН 3. С2Н5ОН 4. С6Н5ОН
19. Продукт взаимодействия фенола с натрием называется:
1. Фенилат натрия 2. Бензоат натрия 3. Фенолят натрия 4. Ацетат натрия
20. Расположите в порядке усиления кислотных свойств:
1) 2-нитрофенол 2) фенол 3) 2,4,6-тринитрофенол 4) 2,4-динитрорфенол
1. 4,3,1,2 2. 3,4,2,1 3. 4,4,1,3 4. 2,1,4,3
21. В водных растворах каких веществ лакмус имеет синий цвет:
1. Уксусная кислота 2. Метилформиат 3. Фенолят калия 4. Глюкоза
22. При взаимодействии этанола массой 92 г с натрием массой 50 г получается газ массой:
1. 2 г 2. 4 г 3. 3 г 4. 1 г
23. Какой объем воздуха потребуется для полного сгорания 2 моль этанола:
1. 44,8 л 2. 134,4 л 3. 640 л 4. 320 л
24. При добавлении избытка бромной воды к 40 мл раствора фенола в этаноле, плотность 0,8 г/мл образовалось 6,62 г осадка. Массовая доля фенола в исходном растворе составляла:
1. 5,88% 2. 4,70% 3. 3,76% 4. 3,12%
Спирты. Фенолы. Вариант № 2
1.К какому классу соединений относится этиленгликоль:
Одноатомные спирты 2. Простые эфиры 3. Многоатомные спирты 4. Альдегиды
2.Какое соединение образуется при взаимодействии этилового спирта и пропановой кислоты:
1. С2Н5СООС2Н5 2. СН3СООС3Н7 3. С3Н7СООС2Н5 4. С3Н7СОС2Н5
3. В схеме превращений С2Н6 → А → С2Н5ОН веществом А является:
1. Хлорэтан или этилен 2. Только этилен 3. Только хлорэтан 4. Ацетальдегид
4. Укажите формулу вещества, которое получается при взаимодействии этанола с хлороводородом:
1. СН3СI 2. CH2CI –CH2CI 3. C2H5CI 4. CH2=CHCI
5. При дегидратации изопропилового спирта образуется:
1. Этилен 2. Ацетилен 3. Пропилен 4. Пропин
6. Качественной реакцией на глицерин является его взаимодействие с:
1. Си(ОН)2 2. Ва(ОН)2 3. Си 4.СН3СООН
7. Функциональная группа спиртов:
1. – СООН 2. – СОН 3. – NH2 4. – ОН
8. Какое вещество получается в результате внутримолекулярной дегидратации этанола:
1. Диэтиловый эфир 2. Этен 3. Диметиловый эфир 4. Этан
9. Уже первый представитель спиртов является жидкостью, это можно объяснить:
1. Большим значением молекулярной массы спиртов 2. Наличием sр2 гибридного атома
3. Наличием водородной связи 4. Способностью спиртов дегидратироваться
10. Каким веществом метанол окисляется в формальдегид:
1. Водородом 2. Натрием 3. Оксидом меди (II) 4. Пероксидом водорода
11. При взаимодействии пропановой кислоты с метанолом в присутствии концентрированной серной кислоты получается вещество, относящееся к классу:
1. Простых эфиров 2. Солей 3. Сложных эфиров 4. Аминокислот
12. К какому классу органических соединений относится карболовая кислота:
1. Спирты 2. Фенолы 3. Альдегиды 4. Карбоновые кислоты
13. Как называется вещество СН3 СН3 СН3 СН3
СН3 – СН – СН — СН —С – СН2ОН
1.2,3,4,5 –тетраметилгексанол-6 2. 2,2,4,5-тетраметилгексанол-1 3. 2,3,4,5-тетраметилгексанол -1 4. 2,3,4,5-тетраэтилгексанол-1
14. В какой паре оба вещества реагируют как с натрием, так и с гидроксидом натрия:
1. Уксусная кислота и фенол 2. Метанол и толуол 3. Этанол и фенол 4. Бензол и этанол
15. Этиловый спирт и глицерин можно различить:
1. Реакцией гидрирования 2. Взаимодействием с гидроксидом меди(II)
3. Взаимодействием с соляной кислотой 4. Взаимодействием с бромной водой
16. Укажите число ὅ — связей в молекуле фенола:
1. 12 2. 11 3. 15 4. 13
17. Укажите пару веществ, которые смешиваются друг с другом ( то есть образуют истинный раствор) в любых соотношениях:
1. Н2О (ж), СаСО3(т) 2. Н2О (ж), С2Н5ОН (ж) 3. Н2О (ж), С6Н6 (ж) 4. Н2О (ж), С6Н5NН2(ж)
18. Расположите в порядке усиления кислотных свойств вещества:
1) Вода 2)Фенол 3)Метанол 4)Уксусная кислота
1. 1,3,2,4 2. 3,1,2,4 3. 2,1,4,3 4. 4,2,1,3
19. В промышленности фенол получают из:
1. Изопропилбензола (кумола) 2. Хлорбензола 3. Бензолсульфокислоты 4. Все ответы верны
20. С какими из перечисленных веществ реагирует фенол:
1) Вода 2) Калий 3) Этанол 4) Азотная кислота 5) Водород 6) Формальдегид
1. 2,3,4,6 2. 1,2,5,6 3. 1,3,4,5 4. 2,4,5,6
21. Какие качества отражают свойства фенола:
1) Бесцветные кристаллы 2) Летучая жидкость 3) Не имеет запаха
4) Имеет характерный запах 5) Хорошо растворяется в воде 6) Ядовит
1. 1,3,5,6 2. 2,4,6 3. 1,4,6 4. 1,4,5,6
22. При взаимодействии предельного одноатомного спирта массой 3,5 г с натрием выделяется газ объемом 0,56 л. Относительная молекулярная масса спирта равна:
1. 70 2. 60 3. 46 4. 88
23. Какой объем кислорода потребуется для получения 1454,7 кДж энергии если тепловой эффект полного сгорания метанола равен 727, 35 кДж:
1. 134,4 л 2. 67,2 л 3. 44,8 л 4. 160 л
24. Какой объем углекислого газа выделится при сгорании 100 г 92% раствора этилового спирта:
1. 11,2 л 2. 22,4 л 3. 44,8 л 4. 89,6 л
Ответы к тестам «Спирты. Фенолы»
Вариант № 1 Вариант № 2
1 – 3 1 – 3
2 – 3 2 – 1
3 – 2 3 – 1
4 – 1 4 – 3
5 – 1 5 – 3
6 – 1 6 – 1
7 – 4 7 – 4
8 – 1 8 – 2
9 – 4 9 – 3
10 – 1 10 – 3
11 – 3 11 – 3
12 – 2 12 – 2
13 – 2 13 — 3
14 – 2 14 – 1
15 – 3 15 – 2
16 – 1 16 – 1
17 – 2 17 – 2
18 – 4 18 – 2
19 – 3 19 – 2
20 – 4 20 – 4
21 – 3 21 – 3
22 – 2 22 – 1
23 – 3 23 – 1
24 – 1 24 — 4
14.6: Гликоли и глицерин — Chemistry LibreTexts
Цели обучения
- Для описания структуры и использования некоторых распространенных многоатомных спиртов.
Спирты с двумя группами ОН на соседних атомах углерода обычно известны как гликоли. Самым важным из них является 1,2-этандиол (обычное название — этиленгликоль), сладкая, бесцветная, несколько вязкая жидкость.
Другой распространенный гликоль, 1,2-пропандиол, обычно называют пропиленгликолем.Его физические свойства очень похожи на свойства этиленгликоля.
1,2,3-пропантриол, обычно называемый глицерином или глицерином, является наиболее важным тригидрокси спиртом. Как и два гликоля, это сладкая сиропообразная жидкость. Глицерин — продукт гидролиза жиров и масел.
Этиленгликоль является основным ингредиентом многих антифризов для автомобильных радиаторов. Две группы ОН приводят к обширной межмолекулярной водородной связи. Это приводит к высокой температуре кипения — 198 ° C; таким образом, этиленгликоль не выкипает при использовании в качестве антифриза.Он также полностью смешивается с водой. Раствор 60% этиленгликоля в воде замерзает при -49 ° C (-56 ° F) и, таким образом, защищает автомобильный радиатор до этой температуры. Этиленгликоль также используется в производстве полиэфирного волокна и магнитной пленки, используемой в лентах для записывающих устройств и компьютеров.
Для вашего здоровья: гликоли и здоровье человека
Этиленгликоль довольно токсичен. Поскольку он сладкий, домашние животные часто собирают пролитый антифриз с пола гаража или подъездной дороги.{2 -} (водн.) \ Rightarrow CaC_2O_4 (s)} \ nonumber \]
Эти кристаллы вызывают повреждение почек и могут привести к почечной недостаточности и смерти.
Хотя пропиленгликоль по своим физическим свойствам очень похож на этиленгликоль, его физиологические свойства совершенно другие. Пропиленгликоль практически нетоксичен, и его можно использовать в качестве растворителя для лекарств и в качестве увлажняющего агента для пищевых продуктов. Как и другие спирты, пропиленгликоль окисляется ферментами печени.
Однако в данном случае продуктом является ион пирувата, нормальный промежуточный продукт в углеводном обмене.Глицерин, продукт метаболизма жиров, по существу нетоксичен.
Сводка
Гликоли — это спирты с двумя группами ОН на соседних атомах углерода. Глицерин — самый важный тригидрокси спирт.
Упражнения по обзору концепции
Какие функциональные группы в реагенте участвуют в окислении пропиленгликоля до пировиноградной кислоты? Какие новые функциональные группы появляются в продукте?
Оксалат-ион образуется при окислении этиленгликоля.В какой реакции участвует оксалат-ион?
ответов
две группы ОН; кетонная группа и группа карбоновой кислоты
Упражнения
Почему этиленгликоль намного более токсичен для человека, чем пропиленгликоль?
Изобразите структуру каждого соединения.
- 1,5-пентандиол
- пропиленгликоль
Изобразите структуру каждого соединения.
- 1,3-гександиол
- глицерин
ответов
спирт с двумя группами ОН на соседних атомах углерода
- HOCH 2 CH 2 CH 2 CH 2 CH 2 OH
CDC — База данных по безопасности и охране здоровья при чрезвычайных ситуациях: Системный агент: ЭТИЛЕНГЛИКОЛЬ
AIR MATRIXBost RO, Sunshine I [1980]. Анализ этиленгликоля методом газовой хроматографии. J. Anal Toxicol 4 (2): 102-103.
Цао XL, Чжу Дж. [2001]. Метод контроля содержания глимов в воздухе и его применение для измерения выбросов выхлопных газов. Chemosphere 45 (6-7): 911-917.
NIOSH [1996]. NMAM 5523, выпуск 1: Гликоли. В кн .: Руководство по аналитическим методам НИОШ. 4-е изд. Цинциннати, Огайо: У.S. Министерство здравоохранения и социальных служб, Служба общественного здравоохранения, Центры по контролю и профилактике заболеваний, Национальный институт профессиональной безопасности и здоровья, Публикация DHHS (NIOSH) № 94-113.
Пендерграсс С.М. [1999]. Определение гликолей в воздухе: разработка методологии отбора проб и анализа и применение к театральным дымам. Am Ind Hyg Assoc J 60: 452-457.
Поттер В. [1999]. Этиленгликоль Метод PV2024. OSHA Солт-Лейк-Сити, штат Юта: Министерство труда США, Технический центр OSHA в Солт-Лейк-Сити, группа хроматографии.
ВОДАХоуз? P, Chaussard J [1993]. Одновременное определение этиленгликоля, пропиленгликоля, 1,3-бутиленгликоля и 2,3-бутиленгликоля в сыворотке крови и моче человека методом газовой хроматографии на широкополосной колонке. J Chromatogr B: Biomed Appl 619 (2): 251-257.
Kenyon AS, Shi X, Wang Y, Ng WH, Prestridge R, Sharp K [1998]. Простое обнаружение примесей диэтиленгликоля / этиленгликоля в глицерине и сырье на основе глицерина на месте с помощью тонкослойной хроматографии. J AOAC Int 81 (1): 44-50.
Маурер Х. Х., Петерс Ф. Т., Пол Л. Д., Кремер Т. [2001]. Утвержденный газовый хроматографически-масс-спектрометрический анализ для определения антифризов этиленгликоля и диэтиленгликоля в плазме крови человека после пивалилирования с помощью микроволнового излучения. J Chromatogr B: Biomed Appl 754 (2): 401-409.
Нильссон Л., Джонс А.В. [1992]. 2,3-Бутандиол: вещество, потенциально мешающее при анализе этиленгликоля ферментативным методом. Clin Chim Acta 208 (3): 225-229.
Oudhoff KA, Schoenmakers PJ, Kok W.T. [2003].Характеристика полиэтиленгликолей и полипропиленгликолей методами капиллярного зонного электрофореза и мицеллярной электрокинетической хроматографии. J Chromatogr A 985 (1-2): 479-491.
Шимански А., Вырвас Б., Шимановска М., Лукашевский З. [2001]. Определение короткоцепочечных полиэтиленгликолей и этиленгликоля в пробах окружающей среды. Water Res 35 (15): 3599-3604.
Валь А., Азаруаль Н., Имбенотт М., Матье Д., Форзи Дж., Картиньи Б., Вермеерш Дж., Лермитт М. [1998]. Отравление метанолом и этиленгликолем: спектроскопия ЯМР 1H как эффективный клинический инструмент для диагностики и количественной оценки.Токсикология 128 (1): 73-81.
.Пример 14: Токсичность этилен / пропиленгликоля | Экологическая медицина: интеграция недостающего элемента в медицинское образование
Рекомендуемый список для чтения
Gabow PA, Clay K, Sullivan JB, et al. Органические кислоты при отравлении этиленгликолем. Энн Интерн Мед, 1986; 105 (1): 16–20.
Миллер В. Токсичность этиленгликоля. Del Med J 1990; 62 (10): 1267–72.
Фактор SA, Lava NS.Отравление этиленгликолем: новый этап клинического синдрома. Нью-Йорк Стейт Дж. Мед, 1987; 87 (3): 179–80.
Ford M, Голдфранк LR. Спирты и гликоли. В: Rippe JM, Irwin RS, Alpert JS, Fink MP, eds. Медицина интенсивной терапии. 2-е изд. Бостон: Литтл, Браун и Ко, 1991: 1160–73.
Якобсен Д., Девлетт Т.О., Уэбб Р. и др. Отравление этиленгликолем: оценка кинетики и кристаллурии. Am J Med 1988; 94 (1): 145–52.
Jacobsen D, McMartin KE. Отравления метанолом и этиленгликолем: механизмы токсичности, клиника, диагностика и лечение.Med Toxicol 1986; 1 (5): 309–34.
Momont SL, Dahlberg PJ. Отравление этиленгликолем. Wis Med J 1989; 88 (9): 16–20.
Винек К.И., Шинглтон Д.П., Шанор СП. Токсичность этилена и диэтиленгликоля. J. Toxicol Clin Toxicol 1978; 13 (2): 297–324.
Baud FJ, Galliot M, Astier A, et al. Лечение отравления этиленгликолем 4-метилпиразолом внутривенно. N Engl J Med 1988; 319: 97–110.
Cheng JT, Beysolow TD, Kaul G, et al. Удаление этиленгликоля почками и гемодиализом.J. Toxicol Clin Toxicol 1987; 25 (1 и 2): 95–108.
Мальмлунд Х.О., Берг А., Карлман Г. и др. Рекомендации по лечению отравления этиленгликолем на основе анализа двух случаев. J. Toxicol Clin Toxicol 1991; 29 (2): 231–40.
Стокс Дж. Б. III, Ауэрон Ф. Предотвращение повреждения органов при массивном приеме этиленгликоля. JAMA 1980; 243: 2065–6.
Агентство регистрации токсичных веществ и заболеваний. Технический отчет для этиленгликоля / пропиленгликоля [черновик].Атланта: Министерство здравоохранения и социальных служб США, Служба общественного здравоохранения, 1992.
Источники информации
Дополнительную информацию о побочных эффектах этиленгликоля и пропиленгликоля и лечении случаев воздействия этих гликолей можно получить в ATSDR, местных и местных департаментах здравоохранения и университетских медицинских центрах. Примеры из практики экологической медицины: токсичность этилен / пропиленгликоля является одним из серии.Чтобы получить другие публикации из этой серии, воспользуйтесь формой заказа на внутренней стороне задней обложки. По клиническим вопросам обращайтесь в ATSDR, Отдел санитарного просвещения, Офис директора, по телефону (404) 639–6204.
,Перевести граммы этиленгликоля в моль
›› Перевести граммы этиленгликоля в
мольПожалуйста, включите Javascript использовать конвертер величин
›› Дополнительная информация в конвертере величин
Сколько граммов этиленгликоля в 1 моль?
Ответ 62,06784.
Мы предполагаем, что вы конвертируете граммов этиленгликоля и моль .
Вы можете просмотреть более подробную информацию о каждой единице измерения:
молекулярная масса этиленгликоля или
моль
Молекулярная формула этиленгликоля — HOCh3Ch3OH.
Основной единицей СИ для количества вещества является моль.
1 грамм этиленгликоля равен 0,016111403264557 моль.
Обратите внимание, что могут возникать ошибки округления, поэтому всегда проверяйте результаты.
Используйте эту страницу, чтобы узнать, как переводить этиленгликоль в граммы на моль.
Введите свои числа в форму, чтобы преобразовать единицы!
›› Похожие химические формулы
Обратите внимание, что все формулы чувствительны к регистру.
Вы хотели преобразовать одну из этих похожих формул?
граммов HOCh3Ch3OH на моль
граммов HoCh3Ch3OH на моль
›› Таблица перевода граммов этиленгликоля в
моль1 грамм этиленгликоля на моль = 0.01611 моль
10 г этиленгликоля на моль = 0,16111 моль
20 граммов этиленгликоля на моль = 0,32223 моль
30 грамм этиленгликоля на моль = 0,48334 моль
40 г этиленгликоля на моль = 0,64446 моль
50 грамм этиленгликоля на моль = 0,80557 моль
100 грамм этиленгликоля на моль = 1,61114 моль
200 грамм этиленгликоля на моль = 3,22228 моль
›› Хотите другие единицы?
Вы можете произвести обратное преобразование единиц измерения из моль этиленгликоля в граммы или введите другие единицы для преобразования ниже:
›› Общее количество превращений веществ
грамма этиленгликоля на децимоль
граммов этиленгликоля на миллимоль
граммов этиленгликоля на пикомоль
граммов этиленгликоля на киломоль
граммов этиленгликоля на атом
граммов этиленгликоля на микромоль
граммов этиленгликоля на наномоль
граммов на молекулу этиленгликоля
граммов на молекулу этиленгликоля этиленгликоль в сантимоль
›› Подробная информация о расчетах молекулярной массы
В химии вес формулы — это величина, вычисляемая путем умножения атомного веса (в единицах атомной массы) каждого элемента в химической формуле на количество атомов этого элемента, присутствующего в формуле, с последующим сложением всех этих продуктов вместе.
Если формула, используемая для вычисления молярной массы, является молекулярной формулой, вычисленная формула веса является молекулярной массой. Массовое процентное содержание любого атома или группы атомов в соединении можно рассчитать, разделив общий вес атома (или группы атомов) в формуле на вес формулы и умножив на 100.
Атомные веса, используемые на этом сайте, получены от Национального института стандартов и технологий NIST. Мы используем самые распространенные изотопы.Вот как рассчитать молярную массу (средний молекулярный вес), которая основана на изотропно взвешенных средних. Это не то же самое, что молекулярная масса, которая представляет собой массу одной молекулы четко определенных изотопов. Для объемных стехиометрических расчетов мы обычно определяем молярную массу, которую также можно назвать стандартной атомной массой или средней атомной массой.
Определение молярной массы начинается с единиц граммов на моль (г / моль). При расчете молекулярной массы химического соединения он говорит нам, сколько граммов содержится в одном моль этого вещества.Вес формулы — это просто вес в атомных единицах массы всех атомов в данной формуле.
Используя химическую формулу соединения и периодическую таблицу элементов, мы можем сложить атомные веса и вычислить молекулярную массу вещества.
Формула веса особенно полезна при определении относительного веса реагентов и продуктов в химической реакции. Эти относительные веса, вычисленные по химическому уравнению, иногда называют весами по уравнениям.
Часто на этом сайте просят перевести граммы в моль. Чтобы выполнить этот расчет, вы должны знать, какое вещество вы пытаетесь преобразовать. Причина в том, что на конверсию влияет молярная масса вещества. Этот сайт объясняет, как найти молярную массу.
›› Метрические преобразования и др.
ConvertUnits.com предоставляет онлайн калькулятор перевода для всех типов единиц измерения. Вы также можете найти метрические таблицы преобразования для единиц СИ. в виде английских единиц, валюты и других данных.Введите единицу символы, сокращения или полные названия единиц длины, площадь, масса, давление и другие типы. Примеры включают мм, дюйм, 100 кг, жидкая унция США, 6 футов 3 дюйма, 10 стоун 4, кубический см, метры в квадрате, граммы, моль, футы в секунду и многое другое!
,
 В небольшом количестве присутствует в креме для обработки обуви.
В небольшом количестве присутствует в креме для обработки обуви. Этиленгликоль является одним из средств обработки больших помещений. Во время нанесения моющих средств его пары вдыхаются, а при нарушении техники безопасности небольшое количество соединения может попасть в рот. Хотя для отравления этого недостаточно.
Этиленгликоль является одним из средств обработки больших помещений. Во время нанесения моющих средств его пары вдыхаются, а при нарушении техники безопасности небольшое количество соединения может попасть в рот. Хотя для отравления этого недостаточно. Тяжёлые больные теряют сознание.
Тяжёлые больные теряют сознание. При отравлении этиленгликолем пострадавшему обеспечивают физический покой, доступ кислорода.
При отравлении этиленгликолем пострадавшему обеспечивают физический покой, доступ кислорода. При работе с химическими веществами, содержащими этиленгликоль, нужно использовать индивидуальные средства защиты.
При работе с химическими веществами, содержащими этиленгликоль, нужно использовать индивидуальные средства защиты.